Fizikai Szemle 2004/7. 216.o.
BIOLÓGIAI ISMERETEK ÉS SUGÁRVÉDELMI SZABÁLYOZÁS
Köteles György
"Fodor József" Országos Közegészségügyi Központ
Országos "Frédéric Joliot-Curie" Sugárbiológiai és Sugáregészségügyi Kutató Intézete
Az ionizáló sugárzás és a radioizotópok 108-109 évvel ezelőtti feltalálása örömöt okozott, mindenki azt hitte, nagyon fontos eszközökhöz jutott a betegségek kezelésében. Ez így is van azóta is, de hamarosan rádöbbentek, hogy ezek a sugárzások igen veszélyesek, súlyos károkat okozhatnak a szervezetben. A szakmai társadalom reagált: létrehozta azt a bizottságot, amelyik a védelem feltételeit vizsgálja. Ez lett a Nemzetközi Sugárvédelmi Bizottság (ICRP). A széles körű társadalom félelme akkor terebélyesedett, amikor a hirosimai és nagaszaki bombázás eredményeiről értesültek. Ezt fokozta a hidegháborús fenyegetések miatti aggodalom, majd az atomerőművi balesetek Pennsylvaniában és Csernobilban. Azóta a sugárzás, az atom szavak hallatán sokan megrémülnek, anélkül, hogy tudnák miről is van szó. Rendszerint ez a helyzet például a kisebb atomerőművi üzemzavarok bejelentésekor is.
A jelen tanulmány célja a jogos aggodalmakat ápolni, erre felhívni a figyelmet, az indokolatlan aggályoskodásokat pedig csökkenteni. Az indokolatlan szorongás, félelem önmaga is egészségkárosító tényező!
A sugárzás tehát veszélyes, mint a tűz, de mint ahogyan a tűzvédelem teszi lehetővé a tűz elengedhetetlen, biztonságos alkalmazását, úgy a sugárvédelem intézkedik a sugaras technológiák biztonságos alkalmazásáról.
Körülöttünk természetes és mesterséges sugárforrások vannak, ezektől jól ismert, jól mérhető sugárterhelést kapunk, ezek nagyságrendje kijelöli számunkra a "mi a sok és mi a kevés" határait, jogszabályi, szervezeti, műszeres felkészültségünk van a sugárzási viszonyok ellenőrzésére és ha szükséges a munkahelyeken dolgozók és a lakosság megóvására az egészségkárosító sugárterhelésektől.
Az alábbiakban részint a sugárvédelmi határértékek változása, másrészt a jelenlegi biológiai ismeretek szerinti biológiai-egészségi hatásokat kiváltó dózistartományok kerülnek tömör ismertetésre.
A sugárvédelmi határértékek változása
A röntgensugárzás és a rádium felfedezését követő első két évtizedben számtalan sérülés történt, hiszen nem ismerték a hatásokat. Ez különösen csúcsosodott az I. Világháború idején, amikor igen egyszerű, védelem nélküli, hordozható röntgenkészülékeket használtak. A német röntgentársaság már 1913-ban ajánlásokat tett közzé, a brit röntgentársaság 1915-ben realizálta a védelem szükségességét, és 1921-ben erre vonatkozó ajánlásokat fogalmazott meg. A 20-as évek elején más országok is felzárkóztak a sugárvédelmi gondolatkörre, mint Olaszország, Norvégia és a Szovjetunió. Az első hazai Sugárvédelmi Szabályok megfogalmazására 1930-ban kezdődtek törekvések. 1925-ben az I. Nemzetközi Radiológiai Kongresszuson a nemzetközi együttműködés szükségessége vetődött fel. Ennek eredményeképpen megalakult az ICRU és 1928-ban az ICRP (akkori nevén International X-ray and Radium Protection Committee). A Bizottság mintegy 3 és fél oldalas ajánlást adott ki a röntgen- és rádiumexpozícióval szembeni védekezésről, nem fogalmazott meg ugyan határértékeket, de ajánlotta sugaras munkahelyen dolgozóknak a hosszabb szabadságot és a munkaórák csökkentését. Néhány mérföldkő:
|
táblázat |
|
A sugárvédelmi dózishatárértékek változása |
|
év |
foglalkozási |
lakossági |
|
1934 |
toleranciadózis 0,2 r/nap1 |
|
|
1951 |
maximálisan 0,5 r/hét egésztest
megengedhető dózis 1,5 r/hét kezek, karok |
|
|
1955 |
egésztest gonádok,vérképző szervek, mint kritikus szervek 300 rem/hét2 |
|
|
1958 |
kumulált dózisegyenérték 5 rem/év |
kumulált dózisegyenérték 0,5 rem/év
genetikai dózis 5 rem/generáció |
|
1977 |
50 mSv/év dózisegyenérték
500 mSv/év szervekre
300 mSvlév szemlencsére |
5 mSv/év egésztest
50 mSv/év szervekre |
|
1990 |
effektív dózis: 20 mSv/év, öt évre átlagolva
egyenértékdózis:
szemlencsére 150 mSv/év
bőrre 500 mSv/év
kezekre, lábakra 500 mSv/év |
effektív dózis: 1 mSv/év
egyenértékdózis:
szemlencsére 15 mSv/év
bőrre 50 mSv/év |
1
1 r = körülbelül 9 mGy, 0,2 r/munkanap = 500 mGy/év -
2
rem = körülbelül 10 mSv
1934-ben
Zürichi találkozásukon használták először a "toleranciadózis" fogalmát, amit körülbelül 0,2 röntgenben jelöltek meg naponta.
1931-ben
A Népszövetség egy bizottságot küldött ki, amelyik a sugárzással járó kockázatokat és a sugárvédelmet lett volna hivatott tanulmányozni.
1950-ben
Újjászervezték az ICRP-t, International Commission on Radiological Protection, magyarul: Nemzetközi Sugárvédelmi Bizottság (ettől kezdve ezen a néven).
1951-ben
Már megjelentették ajánlásaikat, amelyben a "maximális megengedhető dózis" fogalmát vezették be, amit 0,5 röntgenegységben határoztak meg 1 hétre vonatkozóan egésztest-besugárzás esetére és 1,5 röntgenre a kezekre és karokra. Úgy gondolták ugyanis, hogy az előző határérték, azaz a 0,2 r/nap nagyon közel van a káros hatások valószínű küszöbéhez. Ekkor vezették be először azt az elvet, miszerint "mindent el kell követni, hogy bármilyen ionizáló sugárzás esetén az expozíciót a lehetséges legalacsonyabb szintre kell csökkenteni". Ekkor jelenik meg a relatív biológiai hatékonyság (RBE) és a standard ember fogalma. 11 nuklidra maximálisan megengedhető terhelési értéket adtak meg.
1952-ben
H. Müller a genetikai dózis határérték bevezetését ajánlotta, miszerint a per caput gonád dózis ne legyen több, mint 20 r (kb. 200 mSv). Szerinte ezt nem haladnák meg, ha a foglalkozási dózishatárértéket 0,3 r (kb. 3 mSv) heti értékben szabnák meg.
1955-ben
Bevezették a kritikus szerv fogalmát a gonádokra és a vérképző szervekre és az új határértéket 300 millirem/hét értékben szabták meg. Erre alapozva adták meg immár 90 radionuklidra a maximálisan megengedhető koncentrációt (MPC). Érdekes az a megfogalmazásuk, miszerint "a természetes háttérnél nagyobb sugárzási szintek nem tekinthetők abszolút biztonságosnak... és olyan gyakorlati szintet kell választani a mindenkori sugárbiológiai ismeretek alapján, amelyek kockázata elhanyagolható".
1956-ban
Immár nőtt a lakossági védelemre vonatkozó igény a sztochasztikus hatások kivédéséért. Ajánlották, hogy az ellenőrzött zónán kívüli személyek ne kaphassanak a foglalkozási háttérérték 0,1-nél nagyobb sugárterhelést.
1958-ban
Az ICRP 1. számú közleményében az akkumulált dózis egyenérték fogalmát vezette be, valamint az évi határértéket 5 rem-ben szabta meg.
1965-ben
A 9. számú közlemény vezette be a dóziskorlát fogalmát, ezt a foglalkozási kategóriában évi 5 rem-ben, a lakosság egyedeire 0,5 rem-ben ajánlotta.
1977-ben
A 26. számú közlemény vezette be a rem helyett a sievert elnevezést, az effektív dózisegyenérték fogalmát, a sugárvédelem optimalizálása alapjául, az égészség károsodás (Radiation Health Detriment) fogalmát, a maximálisan megengedhető dózis helyett a dóziskorlát fogalmát. Ez utóbbi a foglalkozási kategóriára 50 mSv lett, a lakosság egyedeire 5 mSv, de úgy ajánlva, hogy hosszú távon átlagosan évi 1 mSv-nél ne legyen nagyobb. Elvetették a kritikus szerv fogalmát. A 30. számú közlemény maximálisan megengedhető koncentráció helyett (MPC) az évi felvételi korlát fogalmát (Annual Limit of Intake) vezették be. 1977-ben az ENSZ Atomsugárzás Hatásait Vizsgáló Tudományos Bizottsága (UNSCEAR) fordította először figyelmét a belső terek radonkoncentrációjára, ami hozzájárul az exponáltak effektív egyenértékdózisához.
1991-ben
A 60. számú közlemény a foglalkozási dóziskorlátot 5 évre átlagolva 100 mSv-ben szabta meg, azaz évente 20 mSv, de 50 mSv-nél nem nagyobb, a lakosság egyedeire pedig évi 1 mSv-ben.
A "toleranciadózis"-tól, a bőrpír kiváltását előidéző dózison át tehát hosszú út volt a mai dóziskorlátértékek bevezetéséig. Kezdetben alapvető szempont volt a determinisztikus hatások elkerülése, majd a sztochasztikus hatások kockázatának csökkentése. Valójában tehát mindig az adott biológiai-sugárbiológiai ismeretek ösztönözték a határértékek változtatását, azaz egyre inkább a csökkentését.
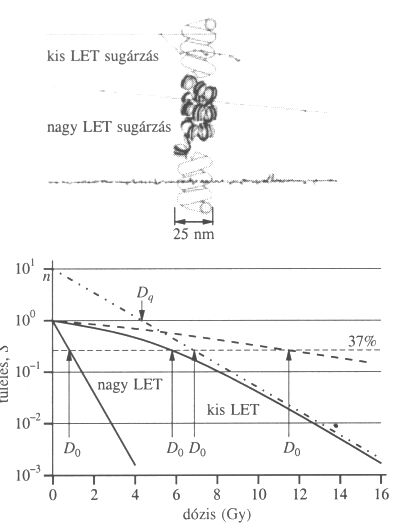
1. ábra. Különböző típusú sugárzások biológiai hatása. Fent: nagy és kis LET-értékű, sűrűn és ritkán ionizáló sugárzások energia átadásának szemléltetése a kromatin-struktúrában. Lent: nagy és kis LET-értékű sugárzások hatása oszló sejtek túlélésére. A túlélő sejtek részaránya (S) logaritmusos skálán, a dózis (D) - lineáris skálán- függvényében ábrázolva (ICRP 1991).
A biológiai-egészségi hatásokat kiváltó dózistartományok
Ionizáló sugárzások biológiai hatását a szervezetben szövetekben, sejtekben - elnyelt energia váltja ki. A hatás mértékét befolyásolja a különböző sugárzások minősége is. Minthogy csak az elnyelődő fotonok, illetve elemi részecskék váltanak ki biológiai reakciót, a rendkívül nagy energiájú és áthatolóképességű és ezért testszövetekben viszonylag kevésbé elnyelődő kemény röntgen- és gamma-fotonok kevésbé hatásosak, mint a nagyszámú iont létrehozó és rövid úthosszon elnyelődő részecske- (alfa, béta-, neutron-) sugárzások.
A lineáris energiaátadás (LET) a részecske haladásának nyomvonalán egységnyi távolságon belül átadott átlagos energia. Egysége: keV/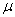 m. Nagy LET-értékű sugárzás esetén a sejtek túlélési görbéje exponenciális lehet, azaz fél-logaritmikus ábrázolásnál lineáris
(1. ábra.) Jellemzője a D0 érték, amely a 37%-os túlélést eredményező dózis. Kis LET-értékű sugárzások - úgynevezett ritkán ionizáló sugárzások -, mint például a röntgensugárzás, a dózishatás görbének a kezdeti szakasza kis dózisoknál kevésbé meredek, mint a nagyobb dózisoknál (1. ábra). Jellemzői az n érték, ami a görbe exponenciális szakaszának és a függőleges tengelynek a metszéspontja és a "kvázi-küszöbdózis" (Dq), annak a görbe exponenciális szakaszának és a 100% túlélési szint vízszintesének metszéspontja. A kis és nagy LET-értékű sugárzások különböző biológiai hatását a relatív biológiai hatékonysággal (RBE) fejezik ki:
m. Nagy LET-értékű sugárzás esetén a sejtek túlélési görbéje exponenciális lehet, azaz fél-logaritmikus ábrázolásnál lineáris
(1. ábra.) Jellemzője a D0 érték, amely a 37%-os túlélést eredményező dózis. Kis LET-értékű sugárzások - úgynevezett ritkán ionizáló sugárzások -, mint például a röntgensugárzás, a dózishatás görbének a kezdeti szakasza kis dózisoknál kevésbé meredek, mint a nagyobb dózisoknál (1. ábra). Jellemzői az n érték, ami a görbe exponenciális szakaszának és a függőleges tengelynek a metszéspontja és a "kvázi-küszöbdózis" (Dq), annak a görbe exponenciális szakaszának és a 100% túlélési szint vízszintesének metszéspontja. A kis és nagy LET-értékű sugárzások különböző biológiai hatását a relatív biológiai hatékonysággal (RBE) fejezik ki:
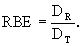
Az RBE a referenciasugárzástól (DR) és bármely más ionizáló sugárzástól származó, ugyanazon biológiai hatás kiváltásához szükséges elnyelt dózisok (DT) hányadosa. Vonatkoztatási sugárzásként a 250 kV röntgen- vagy 60Co gamma-sugárzást alkalmazzák. Az RBE dimenzió nélküli szám, amely megmutatja, hogy a nagy LET-értékű sugárzás hányszor hatásosabb, mint a kis LET-értékű sugárzás. A LET-értékét kísérleti úton lehet meghatározni. Az RBE értéke függ az alkalmazott dózistól, dózisteljesítménytől és a használt biológiai rendszertől.
A fenti sugárbiológiai összefüggések rávilágítanak, arra, hogy a biológiai reagálásoknál a sugárzás fizikai tényezőit is figyelembe kell venni. Az RBE-érték ismeretének jelentőségét pedig éppen egy legutóbbi ICRP közlemény tárgyalja (ICRP92, 2003). A sugárzás okozta biológiai hatások kialakítását számos úgynevezett sugárhatást módosító tényező befolyásolhatja.
Sugárhatást módosító tényezők
Fizikai jellegűek: Sugárhatást módosító tényezőkkel már korábban is, mindig számoltunk. Így a sugárzás LET-értéke, a sugárzás dózisteljesítménye, a besugárzás jellege, azaz akut, krónikus, frakcionált. Maga az ICRP is bevezette a dózis-dózis teljesítménycsökkentő tényező értékét (DDRRF) (ICRP 60, 1991) a sztochasztikus hatások kockázatának becslésében.
A kémiai jellegűekhez az endogén és exogén antioxidáns és sugárvédő vegyületeket soroljuk. E téren az irodalomban az antioxidáns vegyületek és kapacitás feltérképezése folyik.
A biológiai jellegűek között ismert volt néhány sejtélettani jellegzetesség: oszló és nem oszló sejt közötti különbség, vagy a sejt oszlási cikluson belüli helye, a sejtcikluson belüli fázisok szerepe. Újabban e téren halmozódott fel sok ismeret, mint a génaktiválás és -gátlás jelenségei, a sejtciklus szabályozásának szerepe, a sejt-sejt közötti kommunikáció módozatai.
A sugárhatást módosító biológiai tényezők között újabbak is az érdeklődés előterébe kerültek. Ezek közül a kockázatot növelik:
- a gén- és kromoszómainstabilitás kialakulása,
- a közelhatás lehetősége, amikor a "találatot" kapott sejt szomszédjai is sérülnek.
Míg a kockázatot csökkentik:
- az alkalmazkodási válaszreakciók és a kis dózisú sugárzás sejtfolyamatokat stimuláló hatása, hormesis.
A sugárzás sejtszintű biológiai hatásainak komplex ismerete hozzájárul a szervezeti szintű hatások megértéséhez.
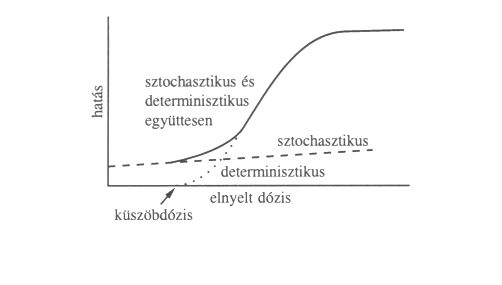
2. ábra. Ionizáló sugárzás sztochasztikus és determinisztikus hatásainak dózis-hatás összefüggése.
A biológiai egészségügyi hatások a mérhető dózisértékekre vonatkoztathatók. A hatások mértékét a dózishatás-összefüggések alapján becsüljük meg. Ez utóbbiak többféle modellel fejezhetők ki. A sugárvédelemben két modell használatos
(2. ábra):
- amikor a sugárzás dózisának növekedésével egy bizonyos biológiai hatás valószínűsége nő, ezek az úgynevezett sztochasztikus hatások, valamint
- amikor a sugárzás dózisának növekedésével egy "küszöbdózis" felett, egy bizonyos hatás súlyossága nő, ezek az úgynevezett determinisztikus hatások.
Sztochasztikus hatások a rosszindulatú daganat keletkezése és az örökletes károsodások. Determinisztikus hatások a szövetek, szervek sérülései, a sugársérülések, a sugárbetegség különböző tünetegyüttesei.
A sztochasztikus hatások közül örökletes hatásokat emberi népességben még nem észleltek. A rákkeletkezés valószínűségére pedig becslések vannak. A legnagyobb vitát az elmúlt években éppen az a kérdés váltotta ki, hogy vajon minden kis dózisnak tulajdonítható-e valamely valószínűség - bármilyen kicsi is -, vagy a sugárhatást módosító fizikai, kémiai tényezők, a biológiai védekezés hatására a kis dózisok kockázata lényegesen kisebb, esetleg elhanyagolható, akár nincs is. Ennek közegészségügyi jelentőségén kívül gyakorlati, pénzügyi jelentősége is van. A kérdés ugyanis az, hogy érdemes-e egyre többet költeni olyan szintű sugárterhelés-csökkentésre a nukleáris energia alkalmazása során, amely az évente természetes forrásoktól eredő terhelésnek ezred-tízezred része.
A determinisztikus hatások balesetek következtében fordulnak elő, ezek ellátására, kezelésére civilizált országokban az egészségügyi szolgálatokat jogszabályok kötelezik.
A kétféle hatáscsoport elkülönítése, az elkülönítés tudatosítása a társadalomban azért is fontos, mert a sugárzáshoz és annak hatásához sok téves elképzelés kapcsolódik. Ez sok indokolatlan félelem forrása. Az egyes sugárzási szinteket és az ezekhez kapcsolható biológiai hatásokat a 3. ábra szemlélteti. Látható, hogy a sztochasztikus, illetve a determinisztikus hatásokat kiváltó dózistartományok több nagyságrenddel különböznek egymástól. Hangsúlyozni kell azt is, hogy míg a determinisztikus hatások orvosi-biológiai módszerekkel diagnosztizálhatók, addig a sztochasztikus hatások az alacsony dózisok tartományában csak epidemiológiai módszerekkel mutathatók ki. Erre alapozta a kockázati tényezőket a Nemzetközi Sugárvédelmi Bizottság (ICRP). A nagy dózisoktól származó megbetegedések gyakoriságából állapította meg a kockázati tényezőket. A kis dózisok felé lineáris extrapolációval lehet egy adott dózistartomány kockázatát megbecsülni. A rosszindulatú daganatos megbetegedésekre vonatkozó becslések emberi népességből származnak. Az örökletes elváltozásokra vonatkozó valószínűség becslése nem emberi populáción történt megfigyelésből származik, hanem sugárbiológiai kísérletekből, a genetikai kutatások különböző vizsgálati alanyaiból a növényektől a kísérleti állatokig.
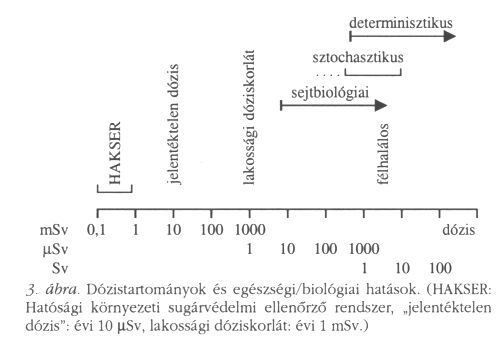
Ami a 3. ábrából szintén nyilvánvaló, hogy a leginkább "rettegett" atomerőművi kibocsátásokból származó sugárterhelések normális működés esetén nagyságrendekkel a természetes háttér alatt vannak. Úgyszintén egyes balesetek, vagy üzemzavari esetek, amire volt példa, a természetes háttérnél lényegesen kisebb többletterhelést jelentettek a hazai lakosságra.
Ki mit tart kis dózisnak?
Az epidemiológiai tanulmányok alapján, a sugárexponált népesség rosszindulatú daganatos betegségeinek statisztikáját feldolgozó és összefoglaló szervezetek a mintegy 200 mSv effektív dózis alatti tartományt kis dózisnak tekintik. Ez az érték úgy adódott, hogy 200 mSv alatt a rákos megbetegedési statisztikák elbizonytalanodnak, nem volt kimutatható szignifikáns összefüggés a dózis és a hatás, illetve a sugárzás indukálta és a nem sugárzás okozta rosszindulatú daganatok gyakorisága között (lásd szaggatott rész sztochasztikus hatások alsó dózistartományában). Bizonyos epidemiológiai felmérések mutattak összefüggést, például pajzsmirigy, emlőrákok, valamint in utero besugárzott magzatok későbbi rosszindulatú megbetegedése eseténél, de a tapasztalatok alapján úgy tűnik, hogy a kis dózisok daganatkeltő hatásaira nem általánosíthatók az ICRP kockázati értékei.
Sejtbiológiailag meglepő módon számos olyan biológiai jelenség érzékelhető, amelyet már 10-100 mSv kivált. Ezt a dózistartományt tekintik a kis dózis tartományának. Sejtszintű elváltozások vizsgálatánál indokolt a mikrodozimetriai megközelítés, amikor az energiaátadást sejtszintű méretekben vizsgálják, a találatok valószínűségét ilyen kis térfogatokra vonatkoztatják. Mikrodozimetriai megközelítésben azt tekintik kis dózisnak, amikor a célponttérfogat 20%-át éri találat. A sejtszintű reagálásoknál hangsúlyozni kell, hogy ezek nem vezetnek feltétlenül károsodásokhoz, hiszen a reagálás, a hibák, elváltozások kijavítását is magába foglalja.
Következtetések
- Az ionizáló sugárzás jól ismert sztochasztikus hatása a rosszindulatú daganatkeltés. A legkisebb dózis, amely statisztikailag szignifikáns módon emeli a kockázatot, 100 mSv körül van. Ez önmagában még nem jelenti küszöbdózis létezését, de arra utal, hogy az egyéb, rákkeltő hatások között ekkora sugárterhelés kockázata eltörpül.
- A mesterséges sugárforrásoktól származó mintegy 1 mSv évenkénti terhelés kockázata a természetes háttér felett, jelenleg nem különböztethető meg a mindennapos, különböző okú egészségkárosító veszélyek között.
- Megfelelő tájékoztatás, gazdasági, környezeti, etikai és pszichológiai ismeretek bővítése szükséges ahhoz, hogy a biztonságos alkalmazás megvalósuljon és azt a társadalom elfogadja éppen a saját jóléte, biztonsága, egészsége és közegészségügye érdekében.
- A kis dózisokkal szembeni aggályoskodás nem szabad, hogy eltérítse a társadalmat az orvosi alkalmazások jótékony hatásainak kihasználásától.
- További kutatások szükségesek a különböző hatások dózis-hatás viszonyainak tanulmányozására, a kisdózisú sugárzás biológiai hatásainak vizsgálatára, a sejtek és a szervezet védekezési és alkalmazkodási mechanizmusainak megismerésére, az exponált emberi közösségek epidemiológiai elemzésének kiterjesztésére, finomítására.
Irodalom
BISZTRAY-BALKU SÁNDOR, BOZÓKY LÁSZLÓ, KOBLINGER LÁSZLÓ: A Sugárvédelem fejlődése Magyarországon - Akadémiai Kiadó, Budapest, 1982
1990 Recommendations of the International Commission on Radiological Protection - ICRP60, Annals of the ICRP, 21, No. 1-3, 1991
Relative biological effectiveness (RBE), quality factor (Q) and radiation weighting factor (WR) - ICRP92, Annals of the ICRP, 2003, Pergamon
B. KANYÁR, G.J. KÖTELES: Dosimetry and biologícal effects of ionizing radiation in "Radiochemistry and radiopharmaceutical chemistry in life sciences" - ed. Rösch, F., Handbook of Nuclear Chemistry, Vol. 4. Chapter 10., Kluwer Acad. Publ., Dordrecht, Boston, London, 2003
KÖTELES GYÖRGY: Ionizáló sugárzás kiváltotta biológiai hatások és közegészségügyi jelentőségük - Egészségtudomány 38 (1994) 195-206
KÖTELES GYÖRGY, TÓTH ESZTER: Gondolatok az ionizáló sugárzás kis dózisainak hatásairól- Fiz. Szle. 49 (1999) 394-400
KÖTELES GYÖRGY: Civilek és szakemberek a nukleáris arénában - Környezetvédelem 2000. XII. 21.
KÖTELES GYÖRGY: A sugáregészségügyről dióhéjban - Tisztiorvos 3 (2000) 11-14
KÖTELES GYÖRGY: Új szempontok a sugárvédelem biológiai alapjaiban - Egészségtudomány 44 (2000) 312-321
KÖTELES GYÖRGY: A csernobili baleset miatt bekövetkezett lakossági sugárterhelés egészségi kockázatai - Orvosi Hetilap 143 (2002) 1411-1414
LÁZÁR ISTVÁN, KÖTELES GYÖRGY: Sugárzás és biológiai rejtélyek - Fiz. Szle. 52 (2002) 151-154
LINDELL BO: A brief history of ICRP - NRPB Radiol Prot. Bull., No. 209, 210, 211 (1999)
Sugáregészségtan (szerk.: Köteles György) - Medicina Kiadó, Budapest, 2002
Sources and effects of ionizing radiation - United Nations, New York, 1993
Sources and effects of ionizing radiation - United Nations, New York, 2000


