Fizikai Szemle 2007/4. 142.o.
MITŐL SZÍNES AZ ÉLŐVILÁG?
Általában hajlamosak vagyunk arra, hogy ami mindennapi
tapasztalat, azt egyszerűen természetes és magától
értetődő dolognak tartsuk. Így van ez a színekkel is.
"A szín a természet mosolya, egy csöppnyi igazság"
- mondta egy angol bölcs. És milyen igaza volt! Mennyivel
kisebb élményt nyújt például a fekete-fehér televízió
és film, mint a színes. Színek nélkül kiüresedne
világunk. Talán fel sem tűnik, de sárga színnel ragyog a
Nap, kék az ég és a tengerek színe, vörös vér kering az
ereinkben, zöld színben pompáznak a lombok, hogy
csak néhányat említsünk. Az egyes színekkel különböző
érzelmi hatást is kiválthatunk. Más színű fénnyel
világítják meg az iskolai tantermet, mással a bárokat, a
húsos pultokat az élelmiszerüzletekben. Tárgyaink a
megvilágító színtől függően más és más színűnek tűnnek,
s bennünk is különböző hatásokat váltanak ki.
A történelem folyamán a színeknek szimbolikus jelentése
is kialakult. Egy időben, Kínában sárga ruhát
csak a császár hordhatott, mert a sárga a legmélyebb
bölcsesség, a legteljesebb megvilágosodás jelképe volt.
A gyászoló kínaiak fehérbe öltöztek, jelezve, hogy az
elhunytat a tisztaság és a fény országába kísérik.
Mást jelentenek a színek a festőknek és a fizikusoknak,
az irodalmároknak, a kémikusoknak, mást a
pszichológusoknak és az ipari formatervezőknek. A
színtan a fizika és az orvosi szakkönyvek önálló fejezetévé
vált. De művészek is könyveket töltenek meg a
színekkel kapcsolatos ismereteikkel.
Mi a magyarázata annak, hogy az égboltot kéknek,
a füvet zöldnek, a paradicsomot pirosnak, a grafitot
feketének látjuk? Mitől színesek a lepkék, a madarak?
Hogy ilyen kérdésekre válaszolhassunk, segítségül
kell hívnunk a fizikát, a kémiát, a biológiát.
A színek
A szín mint jelenség csak részben függ fizikai-kémiai
folyamatoktól. Függ a szem működésétől, s attól is,
hogy mi megy végbe az agyban. A fény érzékelése
összetett, fotokémiai, idegi és pszichológiai folyamatok
eredménye. Az egészséges emberi szem színérzékelése
rendkívül érzékeny, igen sokféle színárnyalatot
képes megkülönböztetni.
A tudósokat már a régmúlt időkből érdekli a különböző
színek eredete. Annak ellenére, hogy a mindennapi
életből és tudományos kísérletekből is rendkívül
sok tapasztalat gyűlt össze a színekről, az eredetükre
vonatkozó kielégítő magyarázatra viszonylag sokáig, a
XVII. századig kellett várni. Newton (1666) előtt a színek
keletkezéséről igen sok, egymásnak ellentmondó magyarázat
forgott közkézen. Igaz, már akkor észrevették,
hogy a testek színe függ a megvilágítástól - ugyanaz a
test a nap különböző szakában más színűnek látszott -,
de a testek színét a testek tulajdonságának vélték.
A szivárvány jelenségét régről ismerik, sőt rögzítették
kialakulásának körülményeit is. Descartes (1596-
1650) szökőkút szétporlasztott vízcseppjein megfigyelt
már mesterséges szivárványt is, sőt ő maga, a
vízcseppet vízzel telt gömb alakú üvegedénnyel modellezve,
a szivárvány színeit kísérletileg is tanulmányozta.
Ennek ellenére a színek keletkezése, azok
sorrendjének oka még akkor sem volt világos.
Newton távcső készítése közben figyelmes lett a lencsék
karimáján vetítéskor megfigyelhető elszíneződésre,
ami érdeklődését a színek tanulmányozásának irányába
fordította. Besötétített szobába vékony nyíláson
beszűrődő fény útjába prizmát helyezett, s a szemközti
falon színes csíkok tűntek fel, elsőként állított elő tehát
színképet. A spektrum elnevezés is tőle származik. A
színkép azt is bizonyította, hogy a fehér fény színes
fény keveréke. Megállapította, hogy a prizma a különböző
színű fénysugarakat különböző módon töri meg
(a jelenséget diszperziónak nevezzük), s ha azokat
lencsével újra összegyűjtjük, ismét fehér fényt kapunk.
A spektrum színei tovább már nem bonthatók.
Newton alapvető kísérlete két fontos felfedezést
tartalmazott:
- ) adott közegben a közeg törésmutatója a különböző
színű fénysugarakra más és más,
- ) a fehér fény egyszerűszínekből összetett fény.
A körülöttünk lévő dolgokat vagy azért látjuk, mert
maguk világítanak, vagy azért, mert megvilágítottuk
őket. A testek a rájuk eső fény egy részét visszaverik
(reflexió), a többit átengedik (transzmisszió) vagy
elnyelik (abszorpció). E három folyamat egymáshoz
viszonyított mértéke határozza meg az önállóan nem
világító testek színét. A fekete színű test például a fény
hullámhosszától függetlenül minden fényt elnyel, az
áttetsző fehér test pedig szinte mindent visszaver. Ha
a fehér fényből valamilyen oknál fogva hiányzik az
egyik összetevő, akkor a megvilágított test a hiányzó
szín kiegészíto (komplementer) színében látszik.
Hogyan állíthatunk elo színeket?
A fény és anyag kölcsönhatásakor az anyagnak átadott
energia függ a fény színétől, a frekvenciájától.
Ha atom vagy molekula nyel el fénykvantumot, megváltozik
a magok és elektronok kölcsönös elrendeződése,
megnövekszik a rendszer energiája. Abból a
tényből, hogy a molekula akármilyen energiát nem
vehet fel, arra következtethetünk, hogy a magok, és
az elektronok rendszere nem lehet tetszőleges állapotban.
Energiájuk csak meghatározott adagokban,
kvantumosan változhat. A rendszernek az állapotváltozáshoz
pontosan meghatározott energiára van
szüksége, s ha ez nem túl nagy energiaadag, akkor
elnyelheti a fényből is. Ha megtörténik az elnyelés,
akkor az atom (vagy molekula) "gerjesztett" állapotba
kerül.
Egy egyszerű mechanikai rendszer, a rezgo húr is
hasonlóan viselkedik. A kifeszített, mindkét végén
rögzített húron állandósult hullámok, állóhullámok
alakulnak ki. A rezgő húrnak is sokféle állandósult
állapota lehet, de nem akármilyen. A rezgő húr is
"kvantumos". A "sokféle, de nem akármilyen állapot"
lehetősége miatt a rezgő húr az atomok és a molekulák,
vagyis az atommagokból és elektronokból álló
rendszerek kitűnő modellje.
Ha gondolatban egy elektront egy L hosszúságú,
minden erőhatástól mentes "egydimenziós dobozba"
zárunk, akkor az elektron mozgásához egy vonalszakasz
áll rendelkezésre. Az elektron az egydimenziós
dobozban szabad, rá semmiféle vonzó vagy taszítóerő
nem hat, helyzeti energiája nincsen. Változhat viszont
a mozgási energiája. Az elektron energiájának az
elektron úgynevezett de Broglie-hullámhosszával való
kapcsolata lehetőséget ad arra, hogy összekapcsoljuk
az elektron lehetséges állapotait a húrmodell el.
Ahogy az L hosszúságú húron csak olyan mozgásállapotok
alakulhatnak ki, amelyekre igaz, hogy a hullámhossz
felének egész számú többszöröse adja a húr
L hosszát, úgy az L hosszúságú vonaldarabra beszorított
elektron mozgási energiája is meghatározott adagokban
változhat. Az energiaadag nagysága fordítottan
arányos a doboz L hosszával. Ez azt jelenti, hogy
ha az elektron mozgásához kellően nagy térrész áll
rendelkezésre, akkor energiáját kis adagokban változtathatja.
Az ilyen "rendszer" már a látható fény viszonylag
kis energiájú fotonjaival is gerjeszthető, s ha
azokat elnyeli, akkor a fehér fény kiegészítő színében
látszik. Ez a modell sikeresen használható festékek
"színezésének" megértéséhez.
Festékek a növény- és állatvilágban
Az élő természet rengeteg színárnyalatát mindössze
háromféle vegyülettípus kialakulása, kölcsönhatása és
bomlása okozza. Ezek a karotinoidok, porfirinek és
flavonoidok. A színek eredetének elemzéséhez ezért
segítségül kell hívnunk a kémiát. A teljesség igénye
nélkül mutatunk néhány példát a környezetünkből
ismert élővilágból minden vegyülettípusra.
A karotinoidok okozzák például az árvácska, a
pitypang virágjának, a sárgarigó és a kanári tollának,
a homár páncéljának a színét. (A hátsó belső borítón
néhány képpel illusztráljuk az élő természet sokszínűségét
az írásban szereplő növények, állatok segítségével.)
A sárgarépa festékanyaga a karotin mellett a
vegyületcsoport egyik legismertebb tagja a likopin.
Likopin legnagyobb mennyiségben a paradicsomban
van, de kevesebb található a csipkebogyóban, a görögdinnyében
és más gyümölcsökben is. Ez a vegyület
felelős a piros színért.
Valamennyi porfirin jellegű festékanyag alapját a
porfin nevű gyűrűs vegyület képezi. A porfirinek két
legfontosabb képviselője a hem és a klorofill. A hem a
vér oxigénszállító molekulája vörös festékanyagának,
a hemoglobinnak a nem fehérjetermészetű része. A
gyűrű középpontjában egy darab két vegyértékű vasatom
van, amely a porfinváz két hidrogénatomját helyettesíti,
és a gyűrűkhöz különböző oldalláncokkal
kapcsolódik. A növények zöld színéért a klorofill a
felelős, ebben a molekulában a porfingyűrű közepén
magnéziumatom található.
A legtöbb virág és gyümölcs a színét a flavonoidoknak
köszönheti. A flavon sárgára színez, a növények
vörös, kék, bordó és ibolya színét pedig az antociánok
okozzák. Az antociánok olyan vegyületek, amelyek egy
színes flavonoid részből és egy színtelen cukorrészből
állnak. Az antociánok a közeg pH-jától függően változtatják
szerkezetüket és ennélfogva a színüket is. Ugyanaz
a vegyület, amely savas közegben (pH = 3) piros,
lúgos közeg (pH = 11) esetén kék, adja a vörös rózsa és
a kék búzavirág színét. Csodálkozunk azon, ha a tavaly
még kék jácint a következő évben vörös színű virágot
hoz. A magyarázat egyszerű. Ha a hangyák véletlenül
tartósan a jácint hagymája körül vernek tanyát, akkor a
hangyasavval savanyított talaj a színekért felelős molekulában
szerkezeti változást idézhet elő. A megváltozott
szerkezetű molekulák a növény szirmára eső fehér
fényből már másik összetevőt nyelnek el, így más kiegészítő
szín mutatkozik. A kertészek ilyen módon a
legváltozatosabb színű virágokat állíthatják elő, például
megfelelő sókat a talajba keverve, mélyen beavatkozhatnak
a természet munkájába.
Vajon mi a közös e szerkezetekben?
Ismeretes, hogy a molekulákban az elektronok 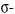 és
és
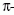 ,
kötő, lazító és nem-kötő molekulapályákon tartózkodnak.
Mindhárom említett szerves molekulatípusban a
molekulában úgynevezett konjugált kettőskötésekkel
szemléltethető elektronelrendezés található. A molekula
lehet lineáris (karotin), de a szénatomok záródhatnak
gyűrűvé is (klorofill). Vagy együtt tartalmazhatnak
hosszabb lineáris szakaszokat és a láncvégeken záródó
gyűrűs elemeket is. Az ilyen molekulákban vannak
olyan elektronok (delokalizált elektronok), amelyek
mozgása a teljes molekulaméretre kiterjedhet. A molekula
hosszában mozgó "szabad" elektronok állapota, és
a két végén rögzített L hosszúságú húr mérete és állapotai
között párhuzamot vonhatunk. A fentiekben már
említett okok miatt a hosszabb molekulában az elektronok
energiája kisebb adagokban változhat, a molekula
kisebb frekvenciájú fény elnyelésére képes. Például a
karotinoidok családjába tartozó, fokozatosan növekvő
számú szénatomot tartalmazó molekulák színe a sárgától
a vörös felé változik. A sárgarépa színe, a karotin a
kék színű fény, a paradicsom vörös színe, a likopin
pedig a zöldessárga színű fény elnyelésével alakul ki. A
piros paprika színéért felelős kapszorubin molekulában
is olyan hosszúságú konjugált lánc található, amely
a zöld fény elnyelését teszi lehetővé, a paprikát a zöld
szín kiegészítő színében, pirosnak látjuk.
,
kötő, lazító és nem-kötő molekulapályákon tartózkodnak.
Mindhárom említett szerves molekulatípusban a
molekulában úgynevezett konjugált kettőskötésekkel
szemléltethető elektronelrendezés található. A molekula
lehet lineáris (karotin), de a szénatomok záródhatnak
gyűrűvé is (klorofill). Vagy együtt tartalmazhatnak
hosszabb lineáris szakaszokat és a láncvégeken záródó
gyűrűs elemeket is. Az ilyen molekulákban vannak
olyan elektronok (delokalizált elektronok), amelyek
mozgása a teljes molekulaméretre kiterjedhet. A molekula
hosszában mozgó "szabad" elektronok állapota, és
a két végén rögzített L hosszúságú húr mérete és állapotai
között párhuzamot vonhatunk. A fentiekben már
említett okok miatt a hosszabb molekulában az elektronok
energiája kisebb adagokban változhat, a molekula
kisebb frekvenciájú fény elnyelésére képes. Például a
karotinoidok családjába tartozó, fokozatosan növekvő
számú szénatomot tartalmazó molekulák színe a sárgától
a vörös felé változik. A sárgarépa színe, a karotin a
kék színű fény, a paradicsom vörös színe, a likopin
pedig a zöldessárga színű fény elnyelésével alakul ki. A
piros paprika színéért felelős kapszorubin molekulában
is olyan hosszúságú konjugált lánc található, amely
a zöld fény elnyelését teszi lehetővé, a paprikát a zöld
szín kiegészítő színében, pirosnak látjuk.
A látás és a színérzet
A karotinhoz nagyon hasonló szerkezetű molekulát, a
retinált (hosszúsága fele a karotinénak) használja
szemünk a fény felfogására, melyhez a szem a hasonló
szerkezetű A-vitaminból jut hozzá. (Ezért okoz az
A-vitamin hiánya szürkületi vakságot). A szemünkbe
érkező fénysugár a különböző színérzékenységű csapokban
(3-féle csap) eltérő erősségű elektromos jelet,
idegáramot idéz elő. Az idegáram-erősségek aránya
minden sugárzás esetén más és más, s az agyban minden
egyes arány esetén más színérzet alakul ki. Ha a
fényinger egyforma erősen hat mind a háromféle
csapra, akkor fehér fényt észlelünk. A vörös fény a
vörösre érzékeny csapokban erősebb idegáramot
kelt, így vörös színérzet keletkezik. Ha a fényinger
egyforma erősen hat a vörösre és a zöldre érzékeny
csapokra, akkor sárga színt látunk. Ily módon valamennyi
szín a vörös, a zöld és a kék keverésével áll
elő. Ezért nevezzük az egészséges színlátást háromszínűnek,
trikromatikusnak, és ezért kell háromszínű
(RGB) jel a színes megjelenítők működtetéséhez.
Szerkezeti színek az élővilágban
A színek a biológiai rendszerekben, a madarak és rovarok
világában gyakran festékszemcsékben, pigmentekben
keletkeznek, a "kémiai színezés"-nél megismert hullámhosszfüggő
fényelnyelés útján. Bizonyos esetekben
azonban a színek keletkezése a fény egy meghatározott
szerkezeten történő szelektív szóródásának, interferenciájának,
illetve diffrakciójának következménye, ezért
ezeket szerkezeti vagy struktúraszíneknek nevezzük.
A természetben gyakran a különböző színezési
lehetőségek kombinálása figyelhető meg. A továbbiakban
néhány példát mutatunk a szerkezeti színeket
"viselő" élőlényekre.
A fényszórás játszik szerepet a kék színnek a kialakításában
a kékszajkó, a kék szem (pl. a sziámi macskáé),
a kékszilva, a kökény esetén. A fényinterferencia
felelős azoknak a színeknek a kialakításáért, amelyek
változnak a megfigyelés irányának (szögének)
változtatásával, s fémes jellegűek. E színeket irizáló
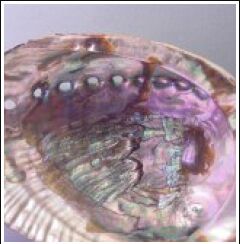
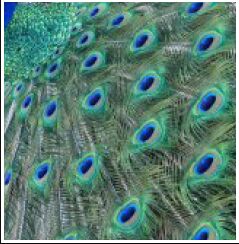
színeknek hívjuk. A kagylóhéjak szivárvány játéka, a
kolibrik ragyogó színei, a pávatoll színének változása,
és néhány Dél-Amerikában élő lepkefaj (Morpho-család)
metálkék színei a legjobb példák e megoldásra. A
fényelhajlás a CD-lemezen élénk spektrum megjelenését
eredményezi, hasonlóan alakul az indigókígyó
színe is bőre finomszerkezetén, amely kétdimenziós
reflexiós diffrakciós rácsként működik.
Rajkovits Zsuzsanna
ELTE Anyagfizikai Tanszék










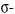 és
és
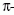 ,
kötő, lazító és nem-kötő molekulapályákon tartózkodnak.
Mindhárom említett szerves molekulatípusban a
molekulában úgynevezett konjugált kettőskötésekkel
szemléltethető elektronelrendezés található. A molekula
lehet lineáris (karotin), de a szénatomok záródhatnak
gyűrűvé is (klorofill). Vagy együtt tartalmazhatnak
hosszabb lineáris szakaszokat és a láncvégeken záródó
gyűrűs elemeket is. Az ilyen molekulákban vannak
olyan elektronok (delokalizált elektronok), amelyek
mozgása a teljes molekulaméretre kiterjedhet. A molekula
hosszában mozgó "szabad" elektronok állapota, és
a két végén rögzített L hosszúságú húr mérete és állapotai
között párhuzamot vonhatunk. A fentiekben már
említett okok miatt a hosszabb molekulában az elektronok
energiája kisebb adagokban változhat, a molekula
kisebb frekvenciájú fény elnyelésére képes. Például a
karotinoidok családjába tartozó, fokozatosan növekvő
számú szénatomot tartalmazó molekulák színe a sárgától
a vörös felé változik. A sárgarépa színe, a karotin a
kék színű fény, a paradicsom vörös színe, a likopin
pedig a zöldessárga színű fény elnyelésével alakul ki. A
piros paprika színéért felelős kapszorubin molekulában
is olyan hosszúságú konjugált lánc található, amely
a zöld fény elnyelését teszi lehetővé, a paprikát a zöld
szín kiegészítő színében, pirosnak látjuk.
,
kötő, lazító és nem-kötő molekulapályákon tartózkodnak.
Mindhárom említett szerves molekulatípusban a
molekulában úgynevezett konjugált kettőskötésekkel
szemléltethető elektronelrendezés található. A molekula
lehet lineáris (karotin), de a szénatomok záródhatnak
gyűrűvé is (klorofill). Vagy együtt tartalmazhatnak
hosszabb lineáris szakaszokat és a láncvégeken záródó
gyűrűs elemeket is. Az ilyen molekulákban vannak
olyan elektronok (delokalizált elektronok), amelyek
mozgása a teljes molekulaméretre kiterjedhet. A molekula
hosszában mozgó "szabad" elektronok állapota, és
a két végén rögzített L hosszúságú húr mérete és állapotai
között párhuzamot vonhatunk. A fentiekben már
említett okok miatt a hosszabb molekulában az elektronok
energiája kisebb adagokban változhat, a molekula
kisebb frekvenciájú fény elnyelésére képes. Például a
karotinoidok családjába tartozó, fokozatosan növekvő
számú szénatomot tartalmazó molekulák színe a sárgától
a vörös felé változik. A sárgarépa színe, a karotin a
kék színű fény, a paradicsom vörös színe, a likopin
pedig a zöldessárga színű fény elnyelésével alakul ki. A
piros paprika színéért felelős kapszorubin molekulában
is olyan hosszúságú konjugált lánc található, amely
a zöld fény elnyelését teszi lehetővé, a paprikát a zöld
szín kiegészítő színében, pirosnak látjuk.











