Fizikai Szemle honlap |
Tartalomjegyzék |
Radnai Gyula
ELTE Általános Fizika Tanszéke
 1872-ben az akkor 50 éves Rudolf Clausius bonni egyetemi tanárt Helmholtz és Kirchhoff társaságában a Magyar
Tudományos Akadémia tiszteleti tagjává választották. Nem mindennapi esemény volt ez: akkor már több mint tíz
éve nem került sor arra, hogy külföldi fizikust a Magyar Tudományos Akadémia tagjai sorába válasszon. (A
Magyar Tudományos Akadémia első fizikus tiszteleti tagja 1847-től Poncelet volt, aki 1829-ben bevezette a
munka egzakt fogalmát.)
Az "áttörést" az európai szemléletű, messzelátó politikus, Eötvös József készítette elő, aki 1867-től (az
osztrák-magyar kiegyezéstől) kezdve 1871-ig (haláláig) egyidejűleg volt vallás- és közoktatásügyi miniszter, s a
Magyar Tudományos Akadémia elnöke. Fiát, Eötvös Lorándot 1868-ban Heidelbergbe küldte egyetemre, ahol
akkor Helmholtz és Kirchhoff tanított. Külföldi tanulmányai során Eötvös Loránd állandó levelezésben állt apjával,
s 1870-ben, amikor hazatért Heidelbergből, az ott summa cum laude doktorátust szerzett ifjú bizonyára
befolyásolta apját elhatározásában, hogy az akkor legnagyobb német fizikusokat hívja meg a Magyar Tudományos
Akadémia tagjai közé (Minisztersége idején Eötvös József nemcsak fiát de számos fiatal tehetséget küldött külföldi
egyetemre, tanulmányutakra. Köztük volt Kármán Mór, a huszadik század egyik világhírű, magyar származású
mérnök-fizikusának Kármán Tódornak az édesapja is. A 26 éves Kármán Mórt azért küldi Lipcsébe Eötvös
József, hogy az ottani tanárképzést tanulmányozza. Két éves tanulmányútján szerzett tapasztalatai alapján szervezte
meg 1871-ben Kármán Mór a budapesti tanárképző intézetet és, a gyakorló gimnáziumot.)
Az 1867-et követő néhány évben a magyar szellemi és tudományos életben érezhető fellendülés következett be, az
európai szellemi áramlatok rendkívül gyorsan hatottak Magyarországon. 1868-ban indította meg az akkor 30 éves
Szily Kálmán a tudományos ismeretterjesztés első magyarországi folyóiratát, a Természettudományi Közlönyt.
Tudományos munkásságában Clausius nyomdokain haladt, Boltzmannhoz hasonlóan Szily Kálmán is a clausiusi
hőelmélet mechanikai megalapozásán dolgozott. Bizonyára neki is szerepe volt abban, hogy Helmoltzon és
Kirchhoffon kívül éppen Clausiust választották meg 1872-ben a Tudományos Akadémia tiszteleti tagjának.
Rudolf Clausius akkor a hőelmélet egyik legnagyobb szaktekintélyének számított a kontinensen. Már hét év telt el
azóta, hogy a második főtétel még világosabb megfogalmazása érdekében bevezetett egy új fizikai mennyiséget,
amelyet entrópiának nevezett el. Valóban, az entrópia bevezetésére Clausiust azok a meg nem értést tükröző, vagy
éppen a második főtétel kimondásában a prioritást vitató írások ösztönözték, amelyek az 1850-es években és a
60-as évek elején jelentek meg. Abban az időben Clausius a gázok kinetikai elméletének kiépítésén dolgozott.
Olyan versenytársai voltnak, mint Maxwell; Clausius 1857-ben publikálta kinetikai gázelméletét, Maxwell 1860-ban
vezette le a gázok sebességeloszlását.
Kénytelen volt azonban időről-időre visszatérni a második főtételnek általa először 1850-ben kimondott
állításához. Az alapvető eszmén semmit sem változtatott, de egyre világosabb és érthetőbb formát keresett
állítása megfogalmazásához. Így jutott el 1865-ben az entrópia fogalmához.
Ahhoz, hogy gondolatmenetét megértsük, szellemi produkcióját kellőképp értékelni tudjuk, bele kell élni magunkat
abba a helyzetbe, amiben Clausius volt 1844-ben, 22 éves korában, miután a berlini egyetemen gimnáziumi tanári
diplomát szerzett.
Szüleinek 18 gyermeke közül Clausius hatodikként született. Édesapja Carl Gottlieb protestáns lelkész és
iskolatanácsos volt, az ő iskolájában tanult Clausius gyermekkorában. Később elvégezte a stetteni gimnázium két
utolsó osztályát; és 1840-ben iratkozott be a berlini egyetemre. Itt matematikát, fizikát, történelmet hallgatott,
többek között Dirichlet, Steiner, Ohm és Magnus voltak a tanárai. A tudomány iránti elhívatottságától vezetve
változtatta meg nevét Gottliebről Clausiusra, ebben is követve a francia felvilágosodás gyakorlatát (gondoljunk
csak például Descartes-Cartesius-ra). Egyetemi évei alatt házitanítóságot is vállalt, hogy keresetével segítse szüleit
a sok gyerek eltartásában. 1844-ben, az egyetem elvégzése után a berlini Friedrich Werder féle gimnáziumba került.
Itt tanított 1850-ig. Ez a hat év - volt Clausius talán legtermékenyebb időszaka, alapvető eszméi ekkor születtek
meg. Szerencsés körülménynek mondható, hogy a hőtan fejlődésében is rendkívül forrongó időszak volt ez,
kiélezett problémákkal, melyek megoldása fiatal, tehetséges koponyákat igényelt.
Clausius, a berlini gimnáziumi tanár, rendszeresen résztvett a berlini fizikai társaság ülésein, előadásain,
bekapcsolódott a vitákba. Itt olvasta fel 1847 június 21-én egy fiatal, 26 éves katonaorvos nevezetes értekezését
"Az erő megmaradásáról", melyben tulajdonképpen az energia megmaradására vonatkozó kísérleti adatait és
elméleti megfontolásait foglalta össze. A katonaorvos Helmholtz volt, aki csak azért végzett katonai orvosi
főiskolát, mert ott ingyenes volt az oktatás, de közben már rendszeresen látogatta Magnus laboratóriumát a
Spree partján. (Az épület - a "Magnus ház" - ma is áll, az NDK Fizikai Társaságának központi épülete,
Helmholtznak pedig szobra áll az egyetem mellett .... )
Helmholtz ismerte Joule 1845-ben publikált méréseit és Robert-Mayer 1842-es eszmefuttatását is. Recsegve-ropogva
omlott össze ezekben az években a hőanyag elmélet, teljesen át kellett értékelni a hőről alkotott addigi elképzeléseket.
A naív materialista szemlélet melynek elterjedését a XVIII. század végi felvilágosodás is segítette azt sugallta,
hogy minden nagy jelenségcsoportban kell találni valamilyen jellegzetes matériát amelynek mennyisége a folyamatok
során változatlan marad. Így vált a tömeg az anyagmennyiség megmaradó mértékévé a kémiai folyamatokban. Így
vezették be a Q töltést mint az elektromosság megmaradó kvantitását az elektromos jelenségek körében.
És így sikerült Blacknek egy mérési utasítással megadható Q hőkvantitást fogalmilag is megkülönböztetni
a hőmérséklettől 1760 körül.
Joule kísérletei most nemcsak arról győztek meg, hogy a Q hőkvantitás nem megmaradó mennyiség,
hanem arról is, hogy a hőmennyiségnek Joule kifejezésével élve - "mechanikai egyenértéke" van, amely munkával
fejezhető ki. A praktikus gondolkodású Joule-t cseppet sem zavarta, hogy eltűnt a fizikából egy megmaradónak
gondolt alapmennyiség. Annál inkább zavarta ez a filozófiailag iskolázottabb Robert Mayert és Helmholtzot, akik
erősen hittek valamilyen ok-, erő-hatásmennyiség megmaradásában, s így jutottak el az energia általános
fogalmához.
Clausiusnak nem okozott gondot Joule és Helmholtz nézeteinek összeegyeztetése, "a mechanikai hőelmélet első
főtételének" megfogalmazása. A későbbiek szempontjából is fontos azonban megjegyezni, hogy Clausius mai
szóhasználattal élve "mechanikai pontrendszert választ modellanyagul". Egyrészt azért választja ezt, mert a
mechanika és a hőelmélet kívánt összekapcsolását ekkor tudja matematikailag is végrehajtani, másrészt azért,
mert végső célja az, hogy a hőelmélet alapegyenleteit mechanikai alaptörvényekből vezesse le. A XIX, század
közepén egy jó fizikai elmélet még egyértelműen a mechanika törvényein kellett hogy alapuljon, ez volt Helmholtz
alapgondolata is.
Clausius így fogalmaz:
" ... Tárgyalásunkban abból a feltevésből akarunk kiindulni, hogy a hő a kisebb test és éterrészecskék mozgásából
áll, a hőmennyiség ezen mozgások eleven erőinek az összege. Ehhez a mozgás természetéről semmiféle
különleges feltevést nem kell tennünk, hanem csak a munkára és az eleven erőre vonatkozó egyenértéktételt,
amely minden mozgásra érvényes, alkalmaznunk kell a hőre is. Az ezáltal keletkező tételt a mechanikai hőelmélet
első főtételének tekintjük."
Másutt ezt írja:
" ... Az eleven erő és a munka egyenértéktételéből levezethető a mechanikai hőelmélet első főtétele, amit a munka
és a hő egyenértéktételének fogunk nevezni."
Az "egyenérték" kifejezés Joule-tól származik, az eleven erő tételének kiterjesztése Helmholtz ötlete.
Már itt, az első főtétel megfogalmazásakor látszik Clausius kiváló képessége a különböző nézetek összeegyeztetésére.
Ez a "rendteremtő" képessége azonban a második főtétel megfogalmazásánál volt igazán segítségére.
Még nem vezették be a fizikában a mechanikai munka egzakt fogalmát, amikor Carnot 1824-ben egy értekezést
publikált "A tűz mozgató erejéről ..." és ebben a hőerőgépekkel végeztethető munkát tette vizsgálat tárgyává.
Carnot dolgozatában az akkor egyik legsürgetőbb kérdésre igyekezett választ adni: van-e elvi határa a gőzgépek
hatásfoka növelésének?
Alapvető elgondolása az volt, hogy a hőerőgépek munkavégzése közben a hő a magasabb hőmérsékletű helyről
az alacsonyabb hőmérsékletű helyre vándorol. Ahogyan a lezúduló víz is képes munkát végezni, miközben a
magasabb helyről az alacsonyabbra jut, úgy végzi a hő is a munkát, miközben a magasabb hőmérsékletű helyekről
az alacsonyabb hőmérsékletű helyekre folyik át. Az analógiát tovább is vitte: ahogyan a víz mennyisége esés
közben változatlan marad, ugyanúgy a hő mennyisége is változatlan marad, miközben munkát végez.
Általánosabban megfogalmazva Carnot gondolatát, azt mondhatjuk, hogy az ő elképzelése szerint a hőmennyiség
úgy áramlik az egyik hőmérsékletű helyről a másikra, mint valamilyen (pl. gravitációs, elektromos, stb.) töltés az
egyik potenciálú helyről a másikra egy konzervatív erőtérben.
Minthogy periodikusan működő gépeket vizsgált, természetesen vezette be a körfolyamat fogalmát, de elméleti
fejtegetéseiben a folyamatok megfordításával is operált. Arra a következtetésre jutott, hogy a kéthőtartályos
körfolyamatok esetén a gép által végzett munka az átáramló hő mennyiségével arányos, s ezen kívül már csak a
két hőmérséklettől függ. A munka és a hő hányadosaként értelmezett hatásfok tehát független a gépben
körfolyamatot végző anyagtól! Carnot bonyolult fejtegetéseihez szemléletes grafikus ábrázolást talált 1834-ben
Clapeyron, akinek nagy szerepe volt abban, hogy Carnot elméleti. meggondolásai nem jutottak a meg nem értett
gondolatok szomorú sorsára, nem kerültek véglegesen a felejtés süllyesztőjébe. Thomson ásta ki újra őket
1847-48-ban, amikor az egyetem elvégzése után egy évig Franciaországban dolgozott.
Az első főtétel megjelenése különös megvilágításba helyezte Carnot elméletét: kiderült, hogy alapfeltevésében
hibás. Mi legyen vele? Ki kell dobni, mint túlhaladottat és tarthatatlant, vagy megmenthető valahogy? Jó lenne
megmenteni egyrészt azért, mert tényleges gyakorlati igényből keletkezett, másrészt azért, mert Thomson
1848-ban Carnot elmélete alapján vezetett be egy olyan univerzális, elvi fontosságú hőmérsékleti skálát, amelynek
segítségével a hőmérséklet mérését hatásfok mérésére - tehát hő és munka mérésére - lehetett visszavezetni.
Igenám, de Carnot szerint a hő munkát tud végezni, Joule szerint a munkából hő nyerhető - és a párizsi akadémia
már 1775 óta nem fogad el perpetuum mobile tervezeteket. De tréfán kívül: a perpetuum mobile lehetetlensége
Carnot érvelésének is egyik sarkalatos pontja volt!
E látszólag kibékíthetetlen ellentmondás feloldása, az ellentétes nézetek összeegyeztetése Clausiusnak való feladat
volt. Gimnáziumi tanári pályájának utolsó évében, 1850-ben publikálta Clausius először a megoldást: a
hőelméletnek két független főtétele van, amelyek azonban nem ellentétesek egymással, hanem két különböző
kérdésre adnak választ.
Joule eredményét, amely szerint a hőnek mechanikai egyenértéke van, Clausius sajátos egyenértéktételnek tekinti,
s úgy fogalmazza meg, hogy "minden esetben, amikor a hő munkát végez, a kifejtett munkával arányos hő fogy
el", s a hő és a munka egyenérték-tételét tekinti a hőtan első főtételének. Ha egy "egyszerű" körfolyamatban
(Clausius így nevezi a Carnot körfolyamatot) "a munkavégző közeg periódusonként Q1
nagyságú T1 hőmérsékletű hőt vesz fel és Q2 nagyságú
T2 hőmérsékletű hőt ad le, akkor Q1-Q2
hővel egyenértékű munkát végez."
Carnot elgondolását, hogy a T1-ről T2-re menő hő mennyisége
változatlan marad, meg lehet menteni, ha csupán a Q2 hőre gondolunk. Clausius nagy ötlete az, hogy a
körfolyamatban kétféle átalakulás játszódik le együttesen: hőnek munkává és hőnek hővé való átalakulása. Ez a két
átalakulás a megfordítható körfolyamatokban "egyenértékű". Későbbi dolgozataiban sikerült Clausiusnak
megadnia azt is, hogyan lehet kiszámítani a "hőből munka", illetve "hőből hő" átalakulások egyenértékeit.
Egyszerű, megfordítható Carnot körfolyamatok esetén:
1872-ben az akkor 50 éves Rudolf Clausius bonni egyetemi tanárt Helmholtz és Kirchhoff társaságában a Magyar
Tudományos Akadémia tiszteleti tagjává választották. Nem mindennapi esemény volt ez: akkor már több mint tíz
éve nem került sor arra, hogy külföldi fizikust a Magyar Tudományos Akadémia tagjai sorába válasszon. (A
Magyar Tudományos Akadémia első fizikus tiszteleti tagja 1847-től Poncelet volt, aki 1829-ben bevezette a
munka egzakt fogalmát.)
Az "áttörést" az európai szemléletű, messzelátó politikus, Eötvös József készítette elő, aki 1867-től (az
osztrák-magyar kiegyezéstől) kezdve 1871-ig (haláláig) egyidejűleg volt vallás- és közoktatásügyi miniszter, s a
Magyar Tudományos Akadémia elnöke. Fiát, Eötvös Lorándot 1868-ban Heidelbergbe küldte egyetemre, ahol
akkor Helmholtz és Kirchhoff tanított. Külföldi tanulmányai során Eötvös Loránd állandó levelezésben állt apjával,
s 1870-ben, amikor hazatért Heidelbergből, az ott summa cum laude doktorátust szerzett ifjú bizonyára
befolyásolta apját elhatározásában, hogy az akkor legnagyobb német fizikusokat hívja meg a Magyar Tudományos
Akadémia tagjai közé (Minisztersége idején Eötvös József nemcsak fiát de számos fiatal tehetséget küldött külföldi
egyetemre, tanulmányutakra. Köztük volt Kármán Mór, a huszadik század egyik világhírű, magyar származású
mérnök-fizikusának Kármán Tódornak az édesapja is. A 26 éves Kármán Mórt azért küldi Lipcsébe Eötvös
József, hogy az ottani tanárképzést tanulmányozza. Két éves tanulmányútján szerzett tapasztalatai alapján szervezte
meg 1871-ben Kármán Mór a budapesti tanárképző intézetet és, a gyakorló gimnáziumot.)
Az 1867-et követő néhány évben a magyar szellemi és tudományos életben érezhető fellendülés következett be, az
európai szellemi áramlatok rendkívül gyorsan hatottak Magyarországon. 1868-ban indította meg az akkor 30 éves
Szily Kálmán a tudományos ismeretterjesztés első magyarországi folyóiratát, a Természettudományi Közlönyt.
Tudományos munkásságában Clausius nyomdokain haladt, Boltzmannhoz hasonlóan Szily Kálmán is a clausiusi
hőelmélet mechanikai megalapozásán dolgozott. Bizonyára neki is szerepe volt abban, hogy Helmoltzon és
Kirchhoffon kívül éppen Clausiust választották meg 1872-ben a Tudományos Akadémia tiszteleti tagjának.
Rudolf Clausius akkor a hőelmélet egyik legnagyobb szaktekintélyének számított a kontinensen. Már hét év telt el
azóta, hogy a második főtétel még világosabb megfogalmazása érdekében bevezetett egy új fizikai mennyiséget,
amelyet entrópiának nevezett el. Valóban, az entrópia bevezetésére Clausiust azok a meg nem értést tükröző, vagy
éppen a második főtétel kimondásában a prioritást vitató írások ösztönözték, amelyek az 1850-es években és a
60-as évek elején jelentek meg. Abban az időben Clausius a gázok kinetikai elméletének kiépítésén dolgozott.
Olyan versenytársai voltnak, mint Maxwell; Clausius 1857-ben publikálta kinetikai gázelméletét, Maxwell 1860-ban
vezette le a gázok sebességeloszlását.
Kénytelen volt azonban időről-időre visszatérni a második főtételnek általa először 1850-ben kimondott
állításához. Az alapvető eszmén semmit sem változtatott, de egyre világosabb és érthetőbb formát keresett
állítása megfogalmazásához. Így jutott el 1865-ben az entrópia fogalmához.
Ahhoz, hogy gondolatmenetét megértsük, szellemi produkcióját kellőképp értékelni tudjuk, bele kell élni magunkat
abba a helyzetbe, amiben Clausius volt 1844-ben, 22 éves korában, miután a berlini egyetemen gimnáziumi tanári
diplomát szerzett.
Szüleinek 18 gyermeke közül Clausius hatodikként született. Édesapja Carl Gottlieb protestáns lelkész és
iskolatanácsos volt, az ő iskolájában tanult Clausius gyermekkorában. Később elvégezte a stetteni gimnázium két
utolsó osztályát; és 1840-ben iratkozott be a berlini egyetemre. Itt matematikát, fizikát, történelmet hallgatott,
többek között Dirichlet, Steiner, Ohm és Magnus voltak a tanárai. A tudomány iránti elhívatottságától vezetve
változtatta meg nevét Gottliebről Clausiusra, ebben is követve a francia felvilágosodás gyakorlatát (gondoljunk
csak például Descartes-Cartesius-ra). Egyetemi évei alatt házitanítóságot is vállalt, hogy keresetével segítse szüleit
a sok gyerek eltartásában. 1844-ben, az egyetem elvégzése után a berlini Friedrich Werder féle gimnáziumba került.
Itt tanított 1850-ig. Ez a hat év - volt Clausius talán legtermékenyebb időszaka, alapvető eszméi ekkor születtek
meg. Szerencsés körülménynek mondható, hogy a hőtan fejlődésében is rendkívül forrongó időszak volt ez,
kiélezett problémákkal, melyek megoldása fiatal, tehetséges koponyákat igényelt.
Clausius, a berlini gimnáziumi tanár, rendszeresen résztvett a berlini fizikai társaság ülésein, előadásain,
bekapcsolódott a vitákba. Itt olvasta fel 1847 június 21-én egy fiatal, 26 éves katonaorvos nevezetes értekezését
"Az erő megmaradásáról", melyben tulajdonképpen az energia megmaradására vonatkozó kísérleti adatait és
elméleti megfontolásait foglalta össze. A katonaorvos Helmholtz volt, aki csak azért végzett katonai orvosi
főiskolát, mert ott ingyenes volt az oktatás, de közben már rendszeresen látogatta Magnus laboratóriumát a
Spree partján. (Az épület - a "Magnus ház" - ma is áll, az NDK Fizikai Társaságának központi épülete,
Helmholtznak pedig szobra áll az egyetem mellett .... )
Helmholtz ismerte Joule 1845-ben publikált méréseit és Robert-Mayer 1842-es eszmefuttatását is. Recsegve-ropogva
omlott össze ezekben az években a hőanyag elmélet, teljesen át kellett értékelni a hőről alkotott addigi elképzeléseket.
A naív materialista szemlélet melynek elterjedését a XVIII. század végi felvilágosodás is segítette azt sugallta,
hogy minden nagy jelenségcsoportban kell találni valamilyen jellegzetes matériát amelynek mennyisége a folyamatok
során változatlan marad. Így vált a tömeg az anyagmennyiség megmaradó mértékévé a kémiai folyamatokban. Így
vezették be a Q töltést mint az elektromosság megmaradó kvantitását az elektromos jelenségek körében.
És így sikerült Blacknek egy mérési utasítással megadható Q hőkvantitást fogalmilag is megkülönböztetni
a hőmérséklettől 1760 körül.
Joule kísérletei most nemcsak arról győztek meg, hogy a Q hőkvantitás nem megmaradó mennyiség,
hanem arról is, hogy a hőmennyiségnek Joule kifejezésével élve - "mechanikai egyenértéke" van, amely munkával
fejezhető ki. A praktikus gondolkodású Joule-t cseppet sem zavarta, hogy eltűnt a fizikából egy megmaradónak
gondolt alapmennyiség. Annál inkább zavarta ez a filozófiailag iskolázottabb Robert Mayert és Helmholtzot, akik
erősen hittek valamilyen ok-, erő-hatásmennyiség megmaradásában, s így jutottak el az energia általános
fogalmához.
Clausiusnak nem okozott gondot Joule és Helmholtz nézeteinek összeegyeztetése, "a mechanikai hőelmélet első
főtételének" megfogalmazása. A későbbiek szempontjából is fontos azonban megjegyezni, hogy Clausius mai
szóhasználattal élve "mechanikai pontrendszert választ modellanyagul". Egyrészt azért választja ezt, mert a
mechanika és a hőelmélet kívánt összekapcsolását ekkor tudja matematikailag is végrehajtani, másrészt azért,
mert végső célja az, hogy a hőelmélet alapegyenleteit mechanikai alaptörvényekből vezesse le. A XIX, század
közepén egy jó fizikai elmélet még egyértelműen a mechanika törvényein kellett hogy alapuljon, ez volt Helmholtz
alapgondolata is.
Clausius így fogalmaz:
" ... Tárgyalásunkban abból a feltevésből akarunk kiindulni, hogy a hő a kisebb test és éterrészecskék mozgásából
áll, a hőmennyiség ezen mozgások eleven erőinek az összege. Ehhez a mozgás természetéről semmiféle
különleges feltevést nem kell tennünk, hanem csak a munkára és az eleven erőre vonatkozó egyenértéktételt,
amely minden mozgásra érvényes, alkalmaznunk kell a hőre is. Az ezáltal keletkező tételt a mechanikai hőelmélet
első főtételének tekintjük."
Másutt ezt írja:
" ... Az eleven erő és a munka egyenértéktételéből levezethető a mechanikai hőelmélet első főtétele, amit a munka
és a hő egyenértéktételének fogunk nevezni."
Az "egyenérték" kifejezés Joule-tól származik, az eleven erő tételének kiterjesztése Helmholtz ötlete.
Már itt, az első főtétel megfogalmazásakor látszik Clausius kiváló képessége a különböző nézetek összeegyeztetésére.
Ez a "rendteremtő" képessége azonban a második főtétel megfogalmazásánál volt igazán segítségére.
Még nem vezették be a fizikában a mechanikai munka egzakt fogalmát, amikor Carnot 1824-ben egy értekezést
publikált "A tűz mozgató erejéről ..." és ebben a hőerőgépekkel végeztethető munkát tette vizsgálat tárgyává.
Carnot dolgozatában az akkor egyik legsürgetőbb kérdésre igyekezett választ adni: van-e elvi határa a gőzgépek
hatásfoka növelésének?
Alapvető elgondolása az volt, hogy a hőerőgépek munkavégzése közben a hő a magasabb hőmérsékletű helyről
az alacsonyabb hőmérsékletű helyre vándorol. Ahogyan a lezúduló víz is képes munkát végezni, miközben a
magasabb helyről az alacsonyabbra jut, úgy végzi a hő is a munkát, miközben a magasabb hőmérsékletű helyekről
az alacsonyabb hőmérsékletű helyekre folyik át. Az analógiát tovább is vitte: ahogyan a víz mennyisége esés
közben változatlan marad, ugyanúgy a hő mennyisége is változatlan marad, miközben munkát végez.
Általánosabban megfogalmazva Carnot gondolatát, azt mondhatjuk, hogy az ő elképzelése szerint a hőmennyiség
úgy áramlik az egyik hőmérsékletű helyről a másikra, mint valamilyen (pl. gravitációs, elektromos, stb.) töltés az
egyik potenciálú helyről a másikra egy konzervatív erőtérben.
Minthogy periodikusan működő gépeket vizsgált, természetesen vezette be a körfolyamat fogalmát, de elméleti
fejtegetéseiben a folyamatok megfordításával is operált. Arra a következtetésre jutott, hogy a kéthőtartályos
körfolyamatok esetén a gép által végzett munka az átáramló hő mennyiségével arányos, s ezen kívül már csak a
két hőmérséklettől függ. A munka és a hő hányadosaként értelmezett hatásfok tehát független a gépben
körfolyamatot végző anyagtól! Carnot bonyolult fejtegetéseihez szemléletes grafikus ábrázolást talált 1834-ben
Clapeyron, akinek nagy szerepe volt abban, hogy Carnot elméleti. meggondolásai nem jutottak a meg nem értett
gondolatok szomorú sorsára, nem kerültek véglegesen a felejtés süllyesztőjébe. Thomson ásta ki újra őket
1847-48-ban, amikor az egyetem elvégzése után egy évig Franciaországban dolgozott.
Az első főtétel megjelenése különös megvilágításba helyezte Carnot elméletét: kiderült, hogy alapfeltevésében
hibás. Mi legyen vele? Ki kell dobni, mint túlhaladottat és tarthatatlant, vagy megmenthető valahogy? Jó lenne
megmenteni egyrészt azért, mert tényleges gyakorlati igényből keletkezett, másrészt azért, mert Thomson
1848-ban Carnot elmélete alapján vezetett be egy olyan univerzális, elvi fontosságú hőmérsékleti skálát, amelynek
segítségével a hőmérséklet mérését hatásfok mérésére - tehát hő és munka mérésére - lehetett visszavezetni.
Igenám, de Carnot szerint a hő munkát tud végezni, Joule szerint a munkából hő nyerhető - és a párizsi akadémia
már 1775 óta nem fogad el perpetuum mobile tervezeteket. De tréfán kívül: a perpetuum mobile lehetetlensége
Carnot érvelésének is egyik sarkalatos pontja volt!
E látszólag kibékíthetetlen ellentmondás feloldása, az ellentétes nézetek összeegyeztetése Clausiusnak való feladat
volt. Gimnáziumi tanári pályájának utolsó évében, 1850-ben publikálta Clausius először a megoldást: a
hőelméletnek két független főtétele van, amelyek azonban nem ellentétesek egymással, hanem két különböző
kérdésre adnak választ.
Joule eredményét, amely szerint a hőnek mechanikai egyenértéke van, Clausius sajátos egyenértéktételnek tekinti,
s úgy fogalmazza meg, hogy "minden esetben, amikor a hő munkát végez, a kifejtett munkával arányos hő fogy
el", s a hő és a munka egyenérték-tételét tekinti a hőtan első főtételének. Ha egy "egyszerű" körfolyamatban
(Clausius így nevezi a Carnot körfolyamatot) "a munkavégző közeg periódusonként Q1
nagyságú T1 hőmérsékletű hőt vesz fel és Q2 nagyságú
T2 hőmérsékletű hőt ad le, akkor Q1-Q2
hővel egyenértékű munkát végez."
Carnot elgondolását, hogy a T1-ről T2-re menő hő mennyisége
változatlan marad, meg lehet menteni, ha csupán a Q2 hőre gondolunk. Clausius nagy ötlete az, hogy a
körfolyamatban kétféle átalakulás játszódik le együttesen: hőnek munkává és hőnek hővé való átalakulása. Ez a két
átalakulás a megfordítható körfolyamatokban "egyenértékű". Későbbi dolgozataiban sikerült Clausiusnak
megadnia azt is, hogyan lehet kiszámítani a "hőből munka", illetve "hőből hő" átalakulások egyenértékeit.
Egyszerű, megfordítható Carnot körfolyamatok esetén:
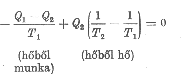
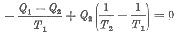
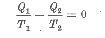
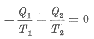
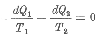
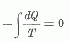
| Az | 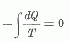 | egyenletet Clausius 1854-ben írta fel először. De csak több mint tíz évvel később, 1865-ben vezette be a |
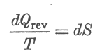
| N = | 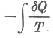 |
| a | 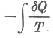 | integrál értéke adja. |
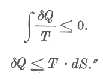
F (T2, T1) = - F (T1, T2). (1)
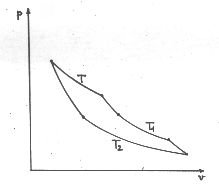
A kapott átalakulási értékeket a fenti ábrával szemléltetett megfordítható körfolyamatra alkalmazva, - ebben a T hőmérsékletű Q hőmennyiség munkává alakul, aminek átalakulási értéke Q& middot; f (T) és Q1 hőmennyiséget pedig T1 hőmérsékletről T2-re vezetünk át, aminek átalakulási egyénértéke Q1 · F (T1,T2), érvényes kell legyen a- Q · f (T) + Q1 · F (T1, T2) = 0 (2)
Az ábrán szemléltetett körfolyamatot fordított irányban úgy hajtsuk végre, hogy a K1 és K2 hőtartályok, valamint a közöttük átvezetett Q1 hő ugyanaz maradjon mint korábban, de a T hőmérsékletű K hőtartály helyett egy másik T' hőmérsékletű K' testet használjunk. Legyen az ebben az esetben a munka árán nyert hő Q', így:Q' · f (T') + Q1 · F (T2 T1) = 0 (3)
- Q · f (T) + Q' · f (T') = 0 (4)
A két egymás után végrehajtott, körfolyamatot tekinthetjük egyetlen körfolyamatnak is. Ebben a K1 és K2 közti hőátmenetek már nem jönnek számításba, kölcsönösen kiegyenlítik egymást, tehát csak a K hőtartályból elvont és munkává alakult Q hőmennyiséget, valamint a munka árán keletkezett és K' által felvett Q' hőmennyiséget kell figyelembe venni. Ez a két ugyanazon jellegű hő → munka átalakulás azonban felbontható két különböző jellegű átalakulásra. Nevezetesen úgy, hogy a Q és Q' hőmennyiségekben közösen meglevő rész minden további nélkül a K testből a K'-be vezetődik át, a fennmaradó rész pedig munkává alakul át (vagy fordítva, attól függően, hogy Q vagy Q' a nagyobb). Legyen a T hőmérséklet nagyobb mint a T', így a hőátvezetés melegebb testből hidegebb test felé irányul, tehát pozitív. Eszerint a másik átalakulás negatív kell legyen, tehát hő alakul át munkává, amiből következik, hogy a K által leadott Q hő nagyobb mint a K' által felvett Q'. Most bontsuk fel gondolatban a Q hőmennyiséget két részre: Q' és Q-Q'-re, ahol az első a K hőtartályból a K'-be átvezetett, utóbbi pedig a munkává átalakult hőmennyiséget jelenti. Ezen felfogás szerint a fent leírt kettős folyamat ugyanolyan jellegű folyamatnak tekinthető, mint azok a folyamatok, amelyekből az összetevődött, tehát a Q' és Q-Q' hőmennyiségekre (2)-höz hasonló összefüggés érvényes:- (Q - Q') · f (T) + Q' · F (T,T') (5)
A (4)-es és (5)-ös egyenletekből egyszerű átalakítások után a következő egyenletet kapjuk:F(T, T') = f (T') - f (T)
Tehát a második fajta átalakulási módra vonatkozó hőmérsékletfüggvény teljesen általánosan visszavezethető az első fajta átalakulási módra érvényes hőmérsékletfüggvényre. Az utóbbi függvény rövidítésére egy egyszerű jelölést veztünk be. Azonban bizonyos okokból célszerű nem magát a függvényt, hanem annak reciprokértékét az új jellel megjelölni:
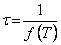
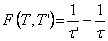
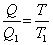
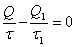
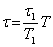
τ = T · constans
s ezáltal a τ hőmérsékletfüggvény egy konstans faktor erejéig meghatározott. A konstans faktor értékeként a legkényelmesebb értéket, az egységet választva:τ = T
Eszerint a τ hőmennyiségfüggvény minden további nélkül az abszolút hőmérséklettel egyenlő. A τ hőmérsékletfüggvény itt levezetett meghatározása a gázokra kapott egyenletekre támaszkodik, így az alkalmazásánál a gázokra tett azon feltevés - miszerint egy ideális gáz, ha konstans hőmérsékleten kitágul, csak annyi hőt vehet fel amennyi külső munkát végez - olyan megszorítás, amelyen a meghatározás alapszik. Ha valakinek ezek miatt kételye támad ezt a meghatározást teljesen megbízhatóként elismerni, akkor az a τ-val jelölt hőmérsékletfüggvényt még ismeretlenkén megtarthatja. Azonban nézetem szerint az ilyen kétely nem indokolt, ezért a továbbiakban τ helyén mindig T áll majd." 1865-ben Clausius már világosan látta, hogy mindkét főtétel egy-egy állapotjelzőt rendel a testhez, és azt is tudta, hogy sem a hő, sem a munka nem lehetnek állapotjelzők. A belső energia fogalmát "molekulárisan" is értelmezte gázokra, az entrópia fogalmához azonban nem fűzött semmilyen molekuláris értelmezést. Hangsúlyozta, hogy az entrópia a test jellemzője, de az entrópia változását úgy értelmezte, mint a reverzibilisen átalakuló hő átalakulási egyenértékét. Clausiusnál még a hőnek is volt hőmérséklete, s a hő átalakulási egyenértéke jelentette az entrópiaváltozást. Nem csoda, hogy az entrópia mikroszkópikus értelmezése a legnagyobb elmék hosszú, fáradságos munkája nyomán született csak meg. Clausius szellemi alkotása még évtizedekig jelentett kihívást a fiatal tehetségek számára. Elég, ha két példát említünk: 1866-ban, egy évvel a clausiusi entrópia megszületése után a 22 éves Boltzmann doktori disszertációjának témájául a második főtételnek mechanikai elvekből való levezetését választotta. 1879-ben, három évvel Clausius összegyűjtött munkáinak első kiadása után a 21 éves Planck doktori disszertációjában a clausiusi második főtételt vetette szigorú kritikai elemzés alá. Mit nyújthat a mai fizikatanár számára a clausiusi entrópiafogalom megismerése? Biztosan segít megérteni, mi köze az entrópiának a szó görög eredetijéhez. Valószínűleg élvezetet okoz megismerni Clausius szintetizáló elméletalkotó módszerét. Lehet, hogy felkelti az érdeklődést Boltzmann, Planck vagy éppen Szily Kálmán kutatásai iránt, melyekhez Clausius alkotása adta az ösztönzést. De jó lenne, ha emellett még növelné a mai középiskolai tanárok alkotókedvét, önbizalmát az a felismerés, hogy az az ember, akiben ezek az ötletek megszülettek, gimnáziumi tanár volt. Igaz, több mint 130 évvel ezelőtt. A felhasznált legfontosabb forrásmunkák: Rudolf Clausius: Die mechanische Wärmetheorie. Braunschweig, 1876.