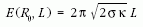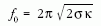Fizikai Szemle 2006/12. B3.o.
MEMBRÁN NANOCSÖVEK
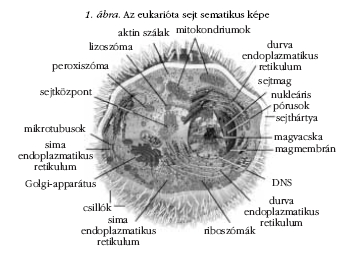
Az élő sejtek felépítésüknél fogva két alapvető csoportra
oszthatók: a sejtmagot nem tartalmazókra (prokariótákra
vagy más néven baktériumokra), valamint a sejtmaggal
rendelkezőkre (eukariótákra, ahová többek között az
összes többsejtű élőlény sejtjei is tartoznak), 1. ábra.
Ezen utóbbi csoport tagjainak további jellegzetessége,
hogy bennük különféle sejtszervecskék találhatók, amelyek
különböző biológiai feladatok ellátására szakosodtak.
A sejtszervecskék általában nagy mennyiségű membránt
(a sejthártyához hasonló felépítésű, néhány nanométer
vastagságú lipid kettősréteget) tartalmaznak, hiszen a
biokémiai feladatokat végző fehérjék jelentős része
membránhoz kötődve működik. Ezek a membránstruktúrák
meglehetősen nagy dinamikus alakváltozásokra képesek
(a sejt életciklusa során vagy külső hatások következtében
nemcsak átrendeződhetnek, de akár időnként
el is tűnhetnek, majd újra felépülhetnek).
Mivel a sejtszervecskékben található membránok összfelülete
több nagyságrenddel is meghaladhatja a sejtfelszínt,
valamiféle kompaktifikációra szorulnak. Erre az
egyik kézenfekvő lehetőség az, hogy a membránok lapos
korong alakú képződmények szorosan pakolt halmazába
rendeződnek (mint pl. az energiaátalakítást végző mitokondriumok
belső membránja, vagy a fehérjék szintéziséért
felelős durva endoplazmatikus retikulum, vagy éppen
a fehérjék osztályozását végző Golgi-apparátus). Egy másik
lehetőség a kompaktifikációra a mindössze néhányszor
tíz nanométer átmérőjű, de akár több mikrométer
hosszúságú nanocsövek kialakítása. Ilyen nanocsövek hálózatából
áll a sima endoplazmatikus retikulum. Nanocsövek
találhatók a Golgi-apparátus bemeneti és kimeneti oldalán
is, de még a sejthártyán is különféle csőszerű
membránkitüremkedések (csillók, állábak stb.) fordulhatnak
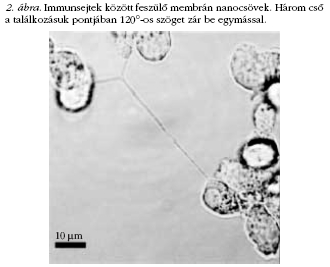
elő. Csak az utóbbi években derült fény arra, hogy bizonyos
típusú sejtek (pl. immunsejtek, agysejtek, vesesejtek)
képesek egymás közt nanocsöveket létrehozni, majd
ezeken keresztül kommunikálni (különböző anyagok
vagy jelek továbbításával), 2. ábra. Mivel a nanocsövek
gyorsabban létrehozhatók, távolabbra elérhetnek és könnyebben
szállíthatók, mint a korong alakú struktúrák, feltehetően
a dinamikusabban változó szerkezetű vagy a
transzportfolyamatokban résztvevő membránstruktúrák
esetén lehetnek hasznosak a sejtek számára.
A membrán nanocsövek kialakulása nagyon egyszerűen
leírható fizikai folyamat. Ezt tekintsük át részletesen a
cikk hátralévő részében. Ehhez elég annyit tudnunk a
membránokról, hogy jól közelíthetők kétdimenziós
összenyomhatatlan (nyújthatatlan) folyadékként. Kétdimenziósként
azért, mert mindössze két vékony lipidrétegből
állnak (amelyben a lipidmolekulák hidrofób farokrésze
a membrán belseje felé, a hidrofil fejrésze pedig
kifelé mutat), 3. ábra, és ezek együttes (tipikusan 4-6
nm) vastagsága messze elmarad a membránfelületek
egyéb jellemző méretétől (pl. a másik két irányú kiterjedésétől
vagy a görbületi sugarától). Összenyomhatatlannak
azért tekinthetjük őket, mert minden egyes lipid molekulára
egy jól meghatározott méretű felületegység jut
(1-2%-nál nagyobb felületváltozást a membrán nem bír
ki). Folyadékként pedig azért kezelhetjük, mert a membrán
síkjában (a sejtek működését lehetővé tevő
hőmérsékleten) a lipidmolekulák szabadon elmozdulhatnak.
A viszkozitásuk egyébként körülbelül
két nagyságrenddel meghaladja a vízét.

Membrán nanocsövek általában erősen
lokalizált húzóerők hatására jönnek létre. Ez
történhet úgy, hogy motorfehérjék (olyan
molekulák, amelyek képesek a sejtváz szálai
mentén haladni) egy kis felületen megragadják
a membránt, és elkezdik a membrán síkjára
merőlegesen húzni, vagy pedig úgy, hogy
polimerizálódó szálak elérik a membránt, és
azt elkezdik nyomni. Már csak az a kérdés,
hogy a lipidmembránoknak milyen fizikai
tulajdonsága teszi lehetővé az ilyen hosszú
cső alakú kitüremkedések kialakulását, hiszen
a hétköznapi tapasztalatunk azt sugallja,
hogy ha egy lapot vagy lepedőt egy pontban megragadva
elkezdünk deformálni, akkor valami kúpszerű képződményt
kapunk. A válasz abban rejlik, hogy a membránok
deformációját alapvetően a következő két rugalmas paraméter
határozza meg: a 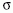 felületi feszültség és
a
felületi feszültség és
a 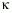 hajlítási
merevség.
Ha ugyanis egy közelítőleg sík alakú membrándarabot
egy pontjában meghúzva deformálunk, akkor ehhez először
is többletfelületre van szükségünk. Mivel a membrán
nyújthatatlan, ezt a többletfelületet vagy a membrán (termikusan
gerjesztett) gyűrődéseinek kisimítása árán szerezhetjük
be, vagy a membrán egy távoli részétől vonhatjuk
el (pl. letapadt felületdarabok felszakításával), vagy a
membránnal esetleg kapcsolatban lévő lipidtartályból
nyerhetjük ki. A lényeg, hogy ehhez energiát kell befektetnünk,
amelynek felületegységre jutó nagyságát jellemzi
a
hajlítási
merevség.
Ha ugyanis egy közelítőleg sík alakú membrándarabot
egy pontjában meghúzva deformálunk, akkor ehhez először
is többletfelületre van szükségünk. Mivel a membrán
nyújthatatlan, ezt a többletfelületet vagy a membrán (termikusan
gerjesztett) gyűrődéseinek kisimítása árán szerezhetjük
be, vagy a membrán egy távoli részétől vonhatjuk
el (pl. letapadt felületdarabok felszakításával), vagy a
membránnal esetleg kapcsolatban lévő lipidtartályból
nyerhetjük ki. A lényeg, hogy ehhez energiát kell befektetnünk,
amelynek felületegységre jutó nagyságát jellemzi
a 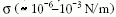 felületi feszültség. Bár ez a paraméter
szoros analógiában áll a közismert határfelületi (pl.
víz-levegő) feszültséggel, a fentiek alapján jól látható,
hogy fizikai eredete egészen más.
Mivel a membrán egy kétdimenziós folyadék, az érintősíkjával
párhuzamos nyírással szemben nem tanúsít
rugalmas ellenállást, csak a síkra merőleges hajlítással
szemben. Ez utóbbit jellemzi a
felületi feszültség. Bár ez a paraméter
szoros analógiában áll a közismert határfelületi (pl.
víz-levegő) feszültséggel, a fentiek alapján jól látható,
hogy fizikai eredete egészen más.
Mivel a membrán egy kétdimenziós folyadék, az érintősíkjával
párhuzamos nyírással szemben nem tanúsít
rugalmas ellenállást, csak a síkra merőleges hajlítással
szemben. Ez utóbbit jellemzi a 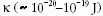 hajlítási
merevség, amely felületegységenként (
hajlítási
merevség, amely felületegységenként (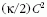 energiával
bünteti a membrán C görbületű meghajlítását.
Hogy egy szemléletes képet kapjunk a nanocsövek
keletkezéséről, először csak a felületi feszültségnek a
felületet csökkentő hatását vegyük figyelembe. A minimális
felülettel jellemzett konfigurációhoz akkor jutnánk
el, amikor a membrán teljesen visszahúzódna az eredeti
síkjába, és a húzási ponthoz már csak egy infinitezimálisan
keskeny (zérus felületet hordozó) szállal kapcsolódna.
Ahogy azonban a membrán kezd ráhúzódni erre a
képzeletbeli szálra (bármilyen is legyen a kiindulási konfiguráció),
a görbülete egyre csak nő. Ekkor válik meghatározó
szerepűvé a hajlítási merevség, amely egy ponton
megállítja az összehúzódást. Az eredmény pedig egy
egyenletes keresztmetszetű cső (a végeitől eltekintve),
amely a membrán síkja és a húzási pont között feszül.
energiával
bünteti a membrán C görbületű meghajlítását.
Hogy egy szemléletes képet kapjunk a nanocsövek
keletkezéséről, először csak a felületi feszültségnek a
felületet csökkentő hatását vegyük figyelembe. A minimális
felülettel jellemzett konfigurációhoz akkor jutnánk
el, amikor a membrán teljesen visszahúzódna az eredeti
síkjába, és a húzási ponthoz már csak egy infinitezimálisan
keskeny (zérus felületet hordozó) szállal kapcsolódna.
Ahogy azonban a membrán kezd ráhúzódni erre a
képzeletbeli szálra (bármilyen is legyen a kiindulási konfiguráció),
a görbülete egyre csak nő. Ekkor válik meghatározó
szerepűvé a hajlítási merevség, amely egy ponton
megállítja az összehúzódást. Az eredmény pedig egy
egyenletes keresztmetszetű cső (a végeitől eltekintve),
amely a membrán síkja és a húzási pont között feszül.
Ennek a csőnek egyszerűen kiszámolhatjuk a sugarát.
Annyit kell csak tennünk, hogy felírjuk egy R sugarú
(vagyis C = 1/R görbületű) és L hosszúságú henger rugalmas
energiáját:
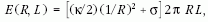
majd minimalizáljuk R szerint. Ebből
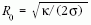
adódik a cső sugarára, amely tipikus paraméterértékek
esetén 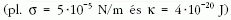 valóban
mindössze néhányszor tíz nanométer nagyságú. Ha most
az R0-ra kapott formulát visszahelyettesítjük a henger
rugalmas energiájába, akkor az
valóban
mindössze néhányszor tíz nanométer nagyságú. Ha most
az R0-ra kapott formulát visszahelyettesítjük a henger
rugalmas energiájába, akkor az
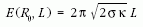
kifejezésből kiolvashatjuk, hogy a nanocsövek
hosszegységenként
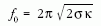
energiát tárolnak, vagyis éppen ekkora húzóerő szükséges
a létrehozásukhoz. Tipikus paraméterértékekre ez tíz pikonewton
körüli erőt jelent, amelynek azért nagy a biológiai
jelentősége, mert már akár egyetlen polimerizálódó
szál vagy néhány molekuláris motorfehérje is képes kifejteni.
Az, hogy a nanocsövek mentén egy ilyen állandó nagyságú
feszítőerő lép fel, jól látszik három cső találkozásánál,
ahol is az erők egyensúlya miatt a csövek úgy állnak be,
hogy egymással páronként 120°-os szöget zárjanak be.
Végezetül érdemes megemlíteni, hogy membrán nanocsöveket
és egész nanocsőhálózatokat mesterségesen
(pl. optikai csipesszel vagy mikropipettával) is elő lehet
állítani. Ezek segítségével tanulmányozhatjuk a membránok
dinamikáját és rugalmas tulajdonságait (pl. különféle
lipidek és membránfehérjék jelenlétében), amelyek nagyon
fontosak a sejtekben található különféle sejtszervecskék
kialakulásának és átrendeződésének megértése szempontjából.
Ugyanakkor a membrán nanocsövek alkalmasak
lehetnek új nanotechnológiai eljárások kidolgozására
is, például nagyon kis mennyiségű folyadékok jól kontrollált
módon történő mozgatására, keverésére. A nanocsövek
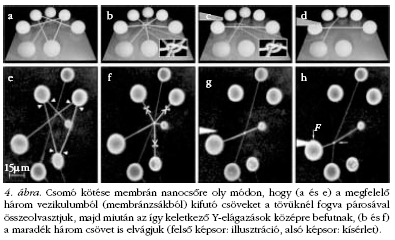
egyébként meglepően stabil struktúrák, még azt is
könnyedén kibírják, ha csomót kötünk rájuk (4. ábra).
Derényi Imre
ELTE, Biológiai Fizika Tanszék

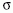 felületi feszültség és
a
felületi feszültség és
a 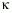 hajlítási
merevség.
Ha ugyanis egy közelítőleg sík alakú membrándarabot
egy pontjában meghúzva deformálunk, akkor ehhez először
is többletfelületre van szükségünk. Mivel a membrán
nyújthatatlan, ezt a többletfelületet vagy a membrán (termikusan
gerjesztett) gyűrődéseinek kisimítása árán szerezhetjük
be, vagy a membrán egy távoli részétől vonhatjuk
el (pl. letapadt felületdarabok felszakításával), vagy a
membránnal esetleg kapcsolatban lévő lipidtartályból
nyerhetjük ki. A lényeg, hogy ehhez energiát kell befektetnünk,
amelynek felületegységre jutó nagyságát jellemzi
a
hajlítási
merevség.
Ha ugyanis egy közelítőleg sík alakú membrándarabot
egy pontjában meghúzva deformálunk, akkor ehhez először
is többletfelületre van szükségünk. Mivel a membrán
nyújthatatlan, ezt a többletfelületet vagy a membrán (termikusan
gerjesztett) gyűrődéseinek kisimítása árán szerezhetjük
be, vagy a membrán egy távoli részétől vonhatjuk
el (pl. letapadt felületdarabok felszakításával), vagy a
membránnal esetleg kapcsolatban lévő lipidtartályból
nyerhetjük ki. A lényeg, hogy ehhez energiát kell befektetnünk,
amelynek felületegységre jutó nagyságát jellemzi
a 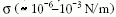 felületi feszültség. Bár ez a paraméter
szoros analógiában áll a közismert határfelületi (pl.
víz-levegő) feszültséggel, a fentiek alapján jól látható,
hogy fizikai eredete egészen más.
Mivel a membrán egy kétdimenziós folyadék, az érintősíkjával
párhuzamos nyírással szemben nem tanúsít
rugalmas ellenállást, csak a síkra merőleges hajlítással
szemben. Ez utóbbit jellemzi a
felületi feszültség. Bár ez a paraméter
szoros analógiában áll a közismert határfelületi (pl.
víz-levegő) feszültséggel, a fentiek alapján jól látható,
hogy fizikai eredete egészen más.
Mivel a membrán egy kétdimenziós folyadék, az érintősíkjával
párhuzamos nyírással szemben nem tanúsít
rugalmas ellenállást, csak a síkra merőleges hajlítással
szemben. Ez utóbbit jellemzi a 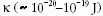 hajlítási
merevség, amely felületegységenként (
hajlítási
merevség, amely felületegységenként (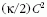 energiával
bünteti a membrán C görbületű meghajlítását.
Hogy egy szemléletes képet kapjunk a nanocsövek
keletkezéséről, először csak a felületi feszültségnek a
felületet csökkentő hatását vegyük figyelembe. A minimális
felülettel jellemzett konfigurációhoz akkor jutnánk
el, amikor a membrán teljesen visszahúzódna az eredeti
síkjába, és a húzási ponthoz már csak egy infinitezimálisan
keskeny (zérus felületet hordozó) szállal kapcsolódna.
Ahogy azonban a membrán kezd ráhúzódni erre a
képzeletbeli szálra (bármilyen is legyen a kiindulási konfiguráció),
a görbülete egyre csak nő. Ekkor válik meghatározó
szerepűvé a hajlítási merevség, amely egy ponton
megállítja az összehúzódást. Az eredmény pedig egy
egyenletes keresztmetszetű cső (a végeitől eltekintve),
amely a membrán síkja és a húzási pont között feszül.
Ennek a csőnek egyszerűen kiszámolhatjuk a sugarát.
Annyit kell csak tennünk, hogy felírjuk egy R sugarú
(vagyis C = 1/R görbületű) és L hosszúságú henger rugalmas
energiáját:
energiával
bünteti a membrán C görbületű meghajlítását.
Hogy egy szemléletes képet kapjunk a nanocsövek
keletkezéséről, először csak a felületi feszültségnek a
felületet csökkentő hatását vegyük figyelembe. A minimális
felülettel jellemzett konfigurációhoz akkor jutnánk
el, amikor a membrán teljesen visszahúzódna az eredeti
síkjába, és a húzási ponthoz már csak egy infinitezimálisan
keskeny (zérus felületet hordozó) szállal kapcsolódna.
Ahogy azonban a membrán kezd ráhúzódni erre a
képzeletbeli szálra (bármilyen is legyen a kiindulási konfiguráció),
a görbülete egyre csak nő. Ekkor válik meghatározó
szerepűvé a hajlítási merevség, amely egy ponton
megállítja az összehúzódást. Az eredmény pedig egy
egyenletes keresztmetszetű cső (a végeitől eltekintve),
amely a membrán síkja és a húzási pont között feszül.
Ennek a csőnek egyszerűen kiszámolhatjuk a sugarát.
Annyit kell csak tennünk, hogy felírjuk egy R sugarú
(vagyis C = 1/R görbületű) és L hosszúságú henger rugalmas
energiáját:
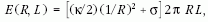
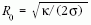
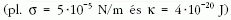 valóban
mindössze néhányszor tíz nanométer nagyságú. Ha most
az R0-ra kapott formulát visszahelyettesítjük a henger
rugalmas energiájába, akkor az
valóban
mindössze néhányszor tíz nanométer nagyságú. Ha most
az R0-ra kapott formulát visszahelyettesítjük a henger
rugalmas energiájába, akkor az